Las células madre son, por decirlo así, como los comodines del cuerpo humano, ya que son capaces de convertirse en cualquier otro tipo de célula, y hasta ahora la forma más sencilla de obtenerlas era extraerlas de embriones, donde son muy abundantes, lo que tiene toda la lógica del mundo, ya que el ser humano completo con todos sus órganos y tejidos diferentes que nace al cabo de los nueve meses de gestación tiene su origen en una sola célula, el cigoto.
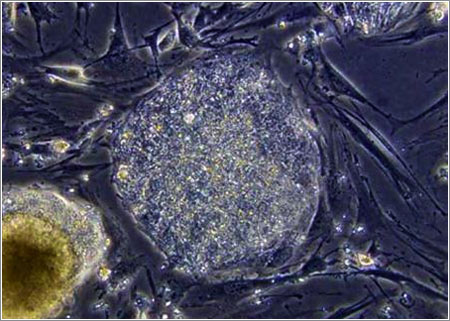
Célula madre no diferenciada
El problema de esto es que para muchos es inmoral utilizar los embriones de esta manera porque extraer esas células supone su destrucción, aunque hay anunciados resultados que afirman que es posible extraer una célula de un embrión de ocho semanas sin que este sufra ningún problema en su desarrollo y obtener un cultivo de células madre a partir de esta célula extraída.
Así, por ejemplo en los Estados Unidos no se puede investigar en este campo con fondos federales, y en la propia Unión Europea la situación varía casi de país a país, y mientras que en España las cosas han ido avanzando en los últimos años, Alemania aún está planteándose suavizar sus leyes al respecto ante el temor expresado por sus científicos de estar quedándose atrás en este campo.
La importancia de las investigaciones con este tipo de células reside en que se piensa que podrían abrir nuevas vías en el tratamiento de enfermedades que van desde la diabetes (Células madre permiten a diabéticos brasileños abandonar la insulina) a la enfermedad de Parkinson (Neuronas de células madre embrionarias frenan el Parkinson en monos) al permitir obtener células de reemplazo para otras dañadas, y también podrían abrir posibilidades increíbles en el campo de los transplantes, ya que podrían servir para cultivar tejidos, y eventualmente órganos, de repuesto para los pacientes que ya no se trataría de que fueran compatibles con su sistema inmune, sino que serían tejidos y órganos de su propio cuerpo.
En esto último, que suena a ciencia ficción, ha habido un par de avances muy interesantes en las últimas semanas.
Por un lado, en Finlandia, a un paciente al que habían tenido que extirparle la mandíbula superior por culpa de un tumor, le pudieron «fabricar» una nueva a partir de células madre extraídas de sus propios tejidos grasos que fueron luego cultivadas en un laboratorio: Finnish patient gets new jaw from own stem cells.
Del cultivo se extrajeron células madre mesenquimales, que son capaces de convertirse en células musculares, de vasos sanguíneos, o de huesos, células que luego fueron implantadas en su propio abdomen junto con una especie de andamio orgánico construido en fosfato de calcio, donde se les dejó crecer durante nueve meses.
Cuando lo extrajeron, el «andamio» estaba rodeado de varios tipos de tejido e incluso de vasos sanguíneos, y una vez implantado en la cabeza del paciente, sujeto en su sitio con tornillos, y conectado a los vasos sanguíneos circundantes usando microcirugía para asegurar su conservación, el paciente ya puede volver a hablar y comer sin necesidad de la prótesis que utilizaba antes.
El otro avance, es la fabricación de un corazón de rata en el laboratorio por parte de científicos de la Universidad de Minnesota, proceso que pudieron llevar a cabo utilizando la estructura inerte de un corazón extraído de una rata muerta en el que tras extraer todas sus células consiguieron hacer crecer tejido cardíaco nuevo a partir de una «papilla» de células de corazón de ratas recién nacidas, papilla rica en células madre y células progenitoras, que son similares a las primeras pero menos flexibles en cuanto a en qué tejidos se pueden convertir.
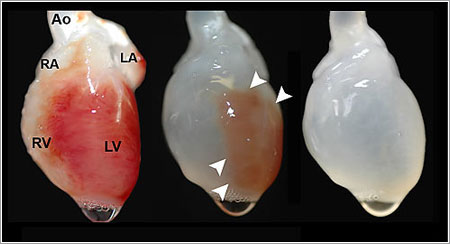
Corazón de rata antes, durante y después del proceso de eliminación de células / Thomas Matthiesen
Obviamente las diferencias entre ratas y humanos son considerables, y aún falta mucho que investigar, pero cuando la doctora Dorys Taylor, que dirige el equipo que creó estos corazones, estuvo en España recientemente, justamente presentando estos resultados, vaticinó que habrá corazones nuevos en cinco años, y siempre sin problemas de rechazo ya que se utilizarían células madre del propio paciente para generar el corazón nuevo.
En este mismo campo, otra noticia reciente de interés es la técnica desarrollada por el equipo de la investigadora María Blasco, del Centro Nacional de Investigaciones Oncológicas (CNIO) y recientemente presentada, que permite teñir secciones de tejido de forma selectiva, de tal modo que las células madre pueden detectarse a simple vista.
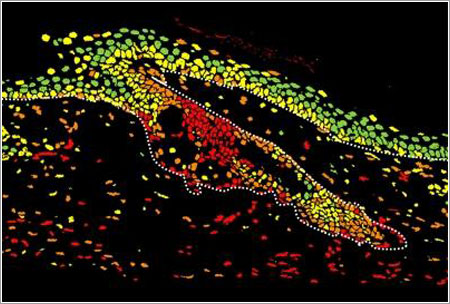
Sección de piel con células madre en rojo / Flores et al
El método de Flores y su equipo se basa en el hecho de que las células madre tienen los telómeros, las secciones de los extremos de sus cromosomas, más largos que otros tipos de células, lo que permite que un marcador fluorescente desarrollado por el equipo para adherirse precisamente a los telómeros haga destacar más estas células que las otras, ya que el marcador tiene más sitio al que agarrarse.
Así, las células madre salen en rojo una vez procesada la imagen, las intermedias en amarillo, y las más viejas en verde.
Para terminar, creo conveniente recordar que todos estos avances están todavía en estado muy experimental, así que aún faltan años para que se puedan aplicar de manera cotidiana, pero ciertamente la impresión es que los avances en este campo se producen a pasos cada vez más agigantados.
No hay comentarios:
Publicar un comentario